Bei fast allen Nierentumoren handelt es sich um sogenannte Nierenzellkarzinome. Diese bösartigen Tumoren (Malignome) sind relativ unempfindlich gegen eine Chemotherapie und können einen sehr unterschiedlichen Verlauf nehmen. Beim Nierenkrebs handelt sich meistens um einen Tumor des älteren Patienten (meist zwischen 60 und 80 Jahren).
Nierenkrebs
Alle hier gegebenen Informationen sind nur allgemeiner Natur, eine Tumortherapie gehört immer in die Hand eines erfahrenen Onkologen!!!
Synonyme
Medizinisch: Nierenzellkarzinom, Hypernephrom
Synonyme im weiteren Sinne: Nierentumor, Nierenkarzinom, Nieren-CA
Englisch: renal cancer, kidney cancer
Definition
Bei fast allen Nierentumoren handelt es sich um sogenannte Nierenzellkarzinome. Diese bösartigen Tumoren (Malignome) sind relativ unempfindlich gegen eine Chemotherapie und können einen sehr unterschiedlichen Verlauf nehmen. Beim Nierenkrebs handelt sich meistens um einen Tumor des älteren Patienten (meist zwischen 60 und 80 Jahren).
Epidemiologie
Jährlich erkranken zwischen 8 und 20 Menschen pro 100.000 Einwohner neu am Nierenkrebs (Nierenkarzinom). Männer sind hier doppelt so häufig betroffen wie Frauen.
Ursachen
Es sind verschiedene Risikofaktoren bekannt, die einen Nierenkrebs (Nieren-CA) begünstigen.
Darunter ist besonders der Tabakkonsum hervorzuheben (v.a. Bei inhalativem Rauchen). Desweiteren scheinen Übergewicht (Adipositas), durch Schmerzmittel (Analgetika) verursachte Nierenschädigungen (Analgetika-Nephropathie), Zystennieren, Dialysebehandlung, Nierentransplantation und das früher zu Röntgenuntersuchungen verwandte Kontrastmittel Thorotrast mit dem Auftreten der Erkrankung in Zusammenhang zu stehen.
Bei den meisten Fällen handelt es sich jedoch um sporadische Nierenzellkarzinome, die von den vererbbaren familiären Formen zu unterscheiden sind.
Man unterscheidet, je nach Aussehen unter dem Mikroskop (histologisch), fünf Formen, je nach dem von welchen Nierenzellen der Tumor seinen Ursprung genommen hat:
- klarzelliges Karzinom (75%): Ausgang vom auskleidenden Gewebe (Epithel) des proximalen Tubulus (siehe auch hierzu die Anatomie der Niere)
- chromophiles Karzinom (15%): Ausgang vom Epithel des proximalen Tubulus (häufig an mehreren Stellen und auf beiden Seiten)
- chromophobes Karzinom (5%): Ausgang vom distalen Tubulusepithel
- onkozytäres Karzinom (3%): Ausgang vom Sammelrohr
- Ductus-Bellini-Karzinom (2%): Ausgang vom Sammelrohr
Anatomie Niere
- Nierenmark
- Nierenrinde
- Nierenarterie
- Nierenvene
- Harnleiter (Ureter)
- Nierenkapsel
- Nierenkelch
- Nierenbecken
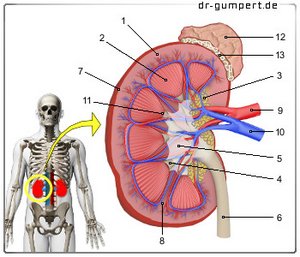
- Nierenrinde - Cortex renalis
- Nierenmark (gebildet von den
Nierenpyramiden) -
Medulla renalis - Nierenbucht (mit Füllfett) -
Sinus renalis - Nierenkelch - Calix renalis
- Nierenbecken - Pelvis renalis
- Harnleiter - Ureter
- Faserkapsel - Capsula fibrosa
- Nierensäule - Columna renalis
- Nierenarterie - A. renalis
- Nierenvene - V. renalis
- Nierenpapille
(Spitze der Nierenpyramide) -
Papilla renalis - Nebenniere -
Glandula suprarenalis - Fettkapsel - Capsula adiposa
Eine Übersicht aller Abbildungen von Dr-Gumpert finden Sie unter: medizinische Abbildungen
Symptome
Da der Nierenkrebs oft für lange Zeit wächst ohne Beschwerden zu verursachen, haben sie bei Diagnosestellung häufig bereits einen Durchmesser von über 5 cm und sind bei ca. 30 % der Patienten schon in den Körper gestreut (metastasiert) und damit die Krankheit nicht mehr heilbar. Wenn sich Krankheitszeichen (Symptome) äußern, dann sind es:
- Blut im Urin (Hämaturie) (bei 40 – 60 %)
- Flankenschmerz (bei 40%)
- tastbare Schwellung (bei 25-45%)
- Gewichtsverlust (bei 30%)
- Blutarmut (Anämie) (bei 30 %)
- Fieber (bei 20%)
Als „klassische Symptomentrias“ bezeichnet man eine Kombination aus den ersten drei Beschwerden. Eine Reihe von Begleiterscheinungen wie zu viele Blutzellen (Polyzythämie), zu viel Kalzium im Blut (Hyperkalziämie) und Beeinträchtigung der Leberfunktion (Stauffer-Syndrom) sind bekannt.
Andere Beschwerden haben ihre Ursache im lokalen Wachstum des Tumors, so z. B. ein Eindringen in die untere Hohlvene (Vena cava inferior) mit Bildung gefährlicher Blutgerinnsel (Thrombose), oder in der Metastasierung (Beschwerden durch Tochtergeschwülste in anderen Geweben, z.B. Rückenschmerzen bei einer Tochtergeschwulst in der Wirbelsäule mit evtl. Wirbelkörperbruch).
Die Tochtergeschwülste (Metastasen) befinden sich bevorzugt in Lungen, Lymphknoten, Leber und Skelett.
Seltener sind Nebennieren, die andere Niere oder das Gehirn befallen. Die meisten betroffenen Patienten haben bei Erkennen der Grunderkrankung (Diagnosestellung) bereits Tochtergeschwülste in mehreren Organen.
Diagnose und Klassifikation
Unvermeidlich zur Erkennung und Stadieneinteilung (sog. Staging) des Nierenkrebs sind die körperliche (klinische) Untersuchung, Ultraschall (Sonographie), Ausscheidungsurographie (beurteilt die Urinausscheidung) und Computertomograpie (CT).
Es gibt zwei gängige Stadieneinteilungen, das TMN-System und die Einteilung nach Robson. Beide richten sich nach der Ausdehnung des Ursprungstumors (Primärtumors), Lymphknoten- oder Fernmetastasen, sowie der Differenzierung des Gewebes (d.h., wenn man das Ursprungsgewebe des Tumors noch ausmachen kann). Das Staging hat Einfluss auf die weitere Therapie und für die Prognose des Patienten.
TMN-Klassifikation nach UICC/WHO (1997)
- T – Primärtumor:
T1 (Tumor auf Niere begrenzt, < 7cm)
T2 (Tumor auf Niere begrenzt, > 7cm)
T3 (Venen- oder Nebenniereninfiltration; Details: a,b,c)
T4 (Infiltration jenseits der Gerota-Faszie)
- N – Regionäre Lymphknoten:
N0 (nicht befallen)
N1 (solitär, regionär)
N2 (> 1 regionärer LK)
N3 (mulitpler Befall, >5cm)
- M – Fernmetastasen:
M0 (keine Fernmetastasen)
M1 (Fernmetastasen; Organcode)
Vor einer Operation kommen noch wahlweise eine Angiographie (Gefäßdarstellung der Arterien), eine Kavograpie (man sieht sich die untere Hohlvene an) und ein MRT vom Bauch hinzu.
Zur Suche nach Metastasen wird eine Röntgenaufnahme des Thorax (Brustkorb) in zwei Ebenen, CT der Lunge, oder ein Skelettszintigramm (Anreicherung radioaktiver Substanzen in Tumorgewebe) angefertigt.
Differentialdiagnosen
Es können auch Nierenzysten für die obengenannten Beschwerden verantwortlich sein.
Dies lässt sich mit bildgebenden Verfahren wie:
- Sonographie (Ultraschall)
- CT (Computertomographie)
- MRT (Magnetresonaztomographie vom Abdomen)
abklären.
Weitere Informationen zum Thema Nierenzysten finden Sie auch unter:
Nierenzysten
Therapie und Prävention
Zur Vermeidung von Nierenzellkarzinomen tragen bei:
- Verzicht auf Rauchen
- Meiden bestimmter Schmerzmittelgruppen (z.B. Phenacetin-haltige Schmerzmittel, z.B. Paracetamol)
- Gewichtsabnahme
- Vorsorgeuntersuchungen bei Patienten mit schwerer Nierenschwäche / Nierenversagen (terminaler Niereninsuffizienz), Zystennieren, von-Hippel-Lindau-Syndrom, tuberöser Sklerose
Bei einem noch nicht gestreuten Nierenzellkarzinom / NIerenkrebs wird als Standardtherapie eine operative Entfernung des Tumors (radikale Tumornephrektomie) mitsamt der Niere, Nebenniere und angrenzenden Lymphknoten angestrebt. Soweit nötig, werden befallene Gefäßanteile mit entfernt und mit einer Gefäßprothese (Ersatzstück für Gefäßanschnitte) versorgt.
Auch bei bereits vorhandenen Tochtergeschwülsten hat die Operation Vorteile: sog. paraneoplastische Symptome (Krankheitszeichen, die nicht direkt durch den Tumor oder dessen Tochtergeschwülste hervorgerufen werden, aber mit dem Auftreten des Tumors in Verbindung stehen; z.B. erhöhte Blutsenkungsgeschwindigkeit 56%, Blutarmut 36%), sowie tumorbedingte Schmerzen und Blutungen werden vermindert. Auch einzelne Metastasen können entfernt werden. Bei Patienten, die von vornherein nur eine Niere haben, wird diese nur teilweise entnommen.
Ein Lokalrezidiv, d. h. ein erneuter Tumor an gleicher Stelle, wird, soweit möglich, erneut entfernt.
Der Nutzen einer adjuvanten Therapie (anschließende Chemo-, Hormon-, Strahelntherapie o.ä.) ist nicht bewiesen. Eingriffe, die nicht eine Heilung, sondern die Linderung der Beschwerden zum Ziel haben (palliative Eingriffe) sind Entfernungen von Metastasen aus Lunge, Hirn und Knochen.
Nierenzellkarzinome reagieren wenig auf Bestrahlung oder Chemotherapie.
Hinweis Behandlung
Neue Behandlungsansätze mit „biological response modifiers“ sind vielversprechend.
Eine neuere Entwicklung ist der Einsatz sogenannter „biological response modifiers“, die in das Immunsystem des Patienten unterstützend eingreifen, um den Tumor zu behandeln.
Es werden Botenstoffe des Immunsystems (Interleukin-2, Tumor-Nekrose-Faktoren) eingesetzt, die das Wachstum der Tumorzellen einschränken und diese als Ziel für zellabtötende (zytotoxische) T-Lymphozyten und Makrophagen (körpereigene Abwehrzellen) makieren. Diese weißen Blutkörperchen (Leukozyten) sorgen dafür, dass die Tumorzellen sich selbst zerstören (Apoptose) oder wirken an der Zerstörung aktiv mit (z.B. durch Phagozytose).
Die positiven Effekte sind aber in der Regel recht kurz und wiegen die beobachteten Nebenwirkungen meistens nicht auf. Zur palliativen Behandlung können sie geeignet sein.
Komplikationen
Sie werden durch das lokale Wachstum des Tumors oder der jeweiligen Metastasen bedingt, so z. B.
Prognose
Das Überleben der Patienten ist in erster Linie vom Tumorstadium abhängig. 60 – 90% der Patienten in Stadium I überleben mind. 5 Jahre, hingegen nur weniger als 20% in Stadium IV.
Ein niedriger Differenzierungsgrad des Tumorgewebes (d.h.: kann man unter dem Mikroskop noch erkennen welche Art von Gewebe entartet ist) und ein schlechter Allgemeinzustand des Patienten wirken sich ebenfalls ungünstig auf die Prognose aus.
Immer wieder wird jedoch über Patienten berichtet, die spontan genesen sind (Spontanremission) oder bei denen die Krankheit jahrelang stabil blieb.
Hier wird ein Einfluss des patienteneigenen Immunsystems vermutet, der zu vielen Behandlungsansätzen geführt hat und vermutlich auch noch führen wird, die auf diese immunologischen Effekte aufbauen.
Weiterführende Informationen
Weiterführende Informationen zu diesem Thema finden Sie unter:
Weitere Themen die für Sie von Interesse sein könnten:
- Niere
- Harnblase
- Harnleiter
- Ableitende Harnwege
- Nierenzysten
- Nierensteine
- Blasenentzündung
- Urologie Online
- Tumor
- Metastase
Alle Themen, die zum Bereich Innere Medizin veröffentlicht wurden, finden Sie unter: