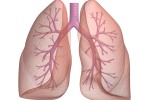
Eine Lungenembolie entsteht aus einem fortgeschwemmten Blutgerinnsel (Thrombose), das eine Lungenarterie verstopft. Dadurch wird der Anteil der Lunge hinter dem Embolus (verstopfender Pfropf) nicht mehr durchblutet. Als Folge steigt der Blutdruck im Lungenkreislauf, wodurch die Leistungsfähigkeit des Herzens kurzfristig überfordert wird.
Inhaltsverzeichnis
- Wie wird eine Lungenembolie therapiert?
- Heparin bei einer Lungenembolie
- Lyse bei einer Lungenembolie
- Operation bei einer Lungenembolie
- Leitliniengerechte Therapie
- Antikoagulation - Blutgerinnungshemmer
- Marcumar®
- Xarelto®
- Clexane®
- Dauer der Therapie
- Therapie einer Lungenembolie in der Schwangerschaft
- Weitere Informationen
Therapie einer Lungenembolie
Bei einer Lungenembolie handelt es sich um eine lebensgefährliche Komplikation eines Blutgerinnsels, das meist aus dem Bein in die Lunge verschleppt wird und dort ein Lungengefäß verschließt.Dadurch wird der Anteil der Lunge hinter dem Gerinnsel nicht mehr durchblutet. Als Folge steigt der Blutdruck im Lungenkreislauf, wodurch die Leistungsfähigkeit des Herzens kurzfristig überfordert wird.
Bei Verdacht auf eine Lungenembolie ist es besonders wichtig, rasch eine Therapie einzuleiten. Hier geht es insbesondere darum, den Thrombus schnellstmöglich aufzulösen und den Kreislauf zu stabilisieren.
Im Folgenden werden Sie über die Therapie bei einer Lungenembolie informiert.
Wir empfehlen Ihnen auch unsere Seiten zu:
Wie wird eine Lungenembolie therapiert?
Im Falle einer akuten Lungenembolie muss zunächst das Gerinnsel aufgelöst werden. Um die Symptome nicht zu verstärken werden die Patienten in sitzender Position gelagert und über eine Nasensonde mit Sauerstoff versorgt. Zudem werden die Patienten sediert und die Schmerzen durch Morphingabe behandelt.
Um den Embolus aufzulösen werden 5.000 bis 10.000 Einheiten Heparin intravenös verabreicht. Injektionen in den Muskel müssen unbedingt vermieden werden. Bei Kreislaufstillstand aufgrund einer Grad 4 Lungenembolie muss sofort eine kardiopulmonale Reanimation mit Herzdruckmassage und Intubation eingeleitet werden. Die spezifische Therapie der Gerinnselauflösung bietet verschiedene Möglichkeiten.
Im Stadium 1 und 2 der Embolie wird der Embolus mit Heparin behandelt. Heparin aktiviert die im Körper vorhandenen hemmenden Faktoren der Gerinnselbildung und potenziert deren Wirkung. Heparin ist damit vor allem prophylaktisch Mittel der Wahl, sofern keine Kontraindikationen vorliegen.
Zudem hat die Lunge selbst eine spontane fibrinolytische Aktivität, und kann den Embolus dadurch innerhalb von Tagen bis Wochen selbst auflösen. Im Stadium 3 und 4 der Lungenembolie wird eine Fibrinolysetherapie eingesetzt. Hierbei wird mittels Streptokinase das körpereigene Plasmin aktiviert. Dieses dient der Auflösung von Gerinnseln und kann damit sowohl den Embolus, als auch den ursprünglichen Thrombus, beispielsweise in den Beinvenen, auflösen.
Neben diesen medikamentösen Methoden der Gerinnselauflösung können auch operative bzw. mechanische Eingriffe zum Einsatz kommen. Indikation für die invasive Gerinnselauflösung sind vor allem Kontraindikationen für die Fibrinolyse.
Hierzu zählen besonders
- vorausgegangene große Operationen in den vergangenen 3 Wochen,
- ein vorangegangener Schlaganfall unklarer Ursache,
- bekannte Blutungsneigungen und
- Blutungen des Magen-Darm-Traktes in den letzten Monaten.
Im Stadium 3 oder 4 einer Embolie kann, bei Kontraindikation für eine Fibrinolyse, der Embolus mittels eines Katheters über das rechte Herz entfernt werden. Die pulmonale Embolektomie ist die letzte Möglichkeit zur Auflösung einer Embolie. Hierbei werden die Patienten an eine Herz-Lungen-Maschine geschlossen und die betroffenen Arterien unter Sicht eröffnet. So lässt sich der Embolus aus der Arterie saugen. Da dieser Eingriff jedoch mit einer Letalität von 25% einhergeht, wird diese Maßnahme nur ergriffen, wenn die anderen Therapieversuche gescheitert sind.
Heparin bei einer Lungenembolie
Heparin ist die Leitsubstanz der nicht-oralen Gerinnungshemmer, das heißt diese Substanz muss zur Verabreichung gespritzt werden.
Es gibt eine Reihe unterschiedlicher Heparine, die sich in ihrer chemischen Struktur unterscheiden und dadurch unterschiedlich lange Wirkzeiten, Applikationswege und Nebenwirkungen haben können.
Der Hauptwirkmechanismus ist dabei bei allen Heparinen gleich, nämlich die Hemmung verschiedener Stufen der körpereigenen Blutgerinnung.
Eine seltene, jedoch wichtige Nebenwirkung, vor allem der unfraktionierten Heparine ist die Heparin-induzierte Thrombozytopenie (kurz: HIT). Dabei kann es zu einer Antikörperbildung kommen, deren Folge ein massiver Abfall der Blutplättchen sein kann.
Daher ist es wichtig, bei der Verabreichung von Heparinen die Blutwerte regelmäßig zu kontrollieren, um weitere mitunter schwerwiegende Komplikationen frühzeitig erkennen und abwenden zu können.
Im Rahmen einer Lungenembolie wird zunächst meist unfraktioniertes Heparin in einer hohen Dosierung eingesetzt, welches intravenös über eine Infusion gegeben werden muss. Im Anschluss daran kann die Therapie auf niedermolekulares Heparin umgestellt werden. Dieses wird subkutan, also unter die Haut gespritzt und wird je nach Körpergewicht und Nierenfunktion unterschiedlich dosiert.
Lyse bei einer Lungenembolie
Je nach Ausmaß der Verlegung von Lungengefäßen durch den Thrombus bei einer Lungenembolie kann das klinische Bild unterschiedlich stark ausgeprägt sein. Handelt es sich dabei um einen vergleichsweise großen Thrombus (Blutgerinnsel), welcher große Teile der Lungenstrombahn blockiert kann die Lungenembolie unter Umständen bis hin zur Reanimationspflicht führen.
In einem solchen Fall kommt es meist zu einer akuten Rechtsherzbelastung, da sich das Blut vor dem Thrombus anstaut und die Herzleistung dies nicht mehr ausreichend kompensieren kann. Man spricht dann von hämodynamischer Instabilität, welche neben der Reanimationspflicht eine Indikation für eine Lysetherapie darstellt.
Dafür wird meist eine Substanz namens Alteplase eingesetzt, welche als Gewebeplasminogenaktivator wirkt. Das Gewebeplasminogen ist dabei ein körpereigenes Molekül, das dabei hilft Thromben wieder aufzulösen. Dieser Prozess wird Fibrinolyse genannt.
Im Rahmen einer Lysetherapie wird dies also pharmazeutisch nachgeahmt, um das blockierte Gefäß möglichst wieder für den Blutstrom freilegen zu können. Parallel dazu sollte eine Antikoagulation (Hemmung der Blutgerinnung) mit Heparin erfolgen, um die Neuentstehung eines Thrombus zu verhindern.
Eine Lysetherapie geht immer mit einem erhöhten Blutungsrisiko einher, weshalb diese ausschließlich unter stationären Bedingungen erfolgen sollte. Darüber hinaus gibt es eine Reihe von Kontraindikationen für eine Lysetherapie. Sobald Reanimationspflicht besteht, treten diese jedoch außer Kraft, da sich der Patient in einem solchen Fall in akuter Lebensgefahr befindet.
Operation bei einer Lungenembolie
Ein operativer Eingriff im Rahmen einer Lungenembolie wird nur selten durchgeführt und ist meist die letzte Therapieoption. Erst wenn andere Therapiemaßnahmen wie Lyse, Antikoagulation und Reanimation versagen kann eine Operation ins Auge gefasst werden.
Diese geht auch wiederum mit einem hohen eigenen Risiko für weitere Komplikationen einher und setzt meist einen guten vorherigen Allgemeinzustand des Patienten voraus. Um den Thrombus operativ entfernen zu können, muss der Herz- Lungen- Kreislauf temporär aus dem Körper ausgelagert werden und durch eine Herz- Lungen- Maschine übernommen werden. In dieser Zeit kann der Operateur dann versuchen, entweder mechanisch mithilfe eines Katheters oder durch eine lokale Lyse den Thrombus zu entfernen.
Leitliniengerechte Therapie
Für die Behandlung einer Lungenembolie gibt es mehrere Leitlinien von unterschiedlichen Fachgesellschaften. Dabei stellen diese lediglich eine Entscheidungshilfe für die behandelnden Ärzte dar, ohne dass sie rechtlich bindend sind.
Sie fassen die aktuelle Studienlage zusammen und lassen diese in das jeweilige Therapieschema einfließen. Je nach klinischem Bild geben sie dann einen Leitfaden für das weitere Procedere an die Hand.
Auch Vor- und Nachteile verschiedener Therapieoptionen können den Leitlinien entnommen werden, um dies bei der individuellen Entscheidung für den jeweiligen Fall mit zu berücksichtigen. In der Regel werden diese Leitlinien alle paar Jahre erneuert und aktualisiert, sodass der aktuelle Stand der Forschung darin festgehalten werden kann.
Auch für besondere Patientenkollektive wie etwa ältere Menschen oder Schwangere werden die wichtigsten Hinweise für deren Therapie in den Leitlinien festgehalten, um auch in „Ausnahmefällen“ nichts zu übersehen.
Die AWMF, die Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V. ist ein Zusammenschluss zahlreicher Fachgesellschaften in Deutschland und eine der größten Plattformen für Leitlinien. Zum Thema „Lungenembolie“ wurde die aktuelle Leitlinie beispielsweise federführend durch die Deutsche Gesellschaft für Angiologie Ende 2015 herausgegeben und ist kostenlos im Internet einsehbar.
Antikoagulation - Blutgerinnungshemmer
Unter Antikoagulation versteht man eine gerinnungshemmende Therapie. Nach einer stattgehabten Lungenembolie sollte medikamentös versucht werden, einem neuen Thrombus entgegenzuwirken, um so einer Lungenembolie vorzubeugen beziehungsweise den bestehenden Thrombus aufzulösen.
Dafür eignet sich die Antikoagulation als Therapieoption, die mithilfe verschiedener Substanzen durchgeführt werden kann. In den meisten Fällen ist eine mindestens dreimonatige Antikoagulation nach einem solchen Ereignis notwendig.
Die bevorzugten Substanzen sind dabei Marcumar®, neue orale direkte Antikoagulatien wie Xarelto® oder niedermolekulare Heparine wie Clexane®. Sie alle hemmen auf unterschiedliche Art und Weise die körpereigene Blutgerinnungskaskade und können dadurch unterschiedliche Wechsel- und Nebenwirkungen aufzeigen.
Das könnte Sie auch interessieren: Wie sehen die Überlebenschancen bei einer Lungenembolie aus?
Marcumar®
Marcumar® ist der Handelsname für Phenprocoumon, einer Substanz welche die Funktion des Vitamin K im Körper hemmt. Vitamin K ist nämlich für die Herstellung verschiedener Bausteine der Gerinnungskaskade in der Leber notwendig - gibt es kein funktionstüchtiges Vitamin K so können auch die Gerinnungsfaktoren nicht gebildet werden und die Blutgerinnung ist gestört.
Da die Herstellung dieser Gerinnungsfaktoren in der Regel mehrere Tage in Anspruch nimmt, ist Marcumar® als Medikament insgesamt relativ schlecht steuerbar und bedarf regelmäßigen Kontrollen der Blutgerinnungsaktivität. Dafür wird meist der INR (engl. International Normalized Ratio) bestimmt, ein Wert der Aufschluss über das Ausmaß der Gerinnungshemmung geben kann. Nach einer Lungenembolie wird meist ein Wert zwischen 2 und 3 langfristig angestrebt.
Bei dauerhafter Marcumareinnahme gilt es zudem zu beachten, dass es Wechselwirkungen zwischen diesem Medikament und anderen Medikamenten und sogar Lebensmitteln geben kann. Diese können sowohl zu einer Wirkungsverstärkung mit erhöhtem Blutungsrisiko als auch zu einer Wirkungsabschwächung mit erhöhter Thrombosegefahr führen. Und nicht zuletzt sollte Marcumar® vor operativen Eingriffen aufgrund der besseren Steuerbarkeit rechtzeitig auf Heparin umgestellt werden.
Xarelto®
Xarelto® ist der Handelsname für eine Substanz namens Rivaroxaban. Diese wird zu der Gruppe der neuen oralen Antikoagulantien gezählt und hemmt die körpereigene Blutgerinnung. Im Gegensatz zum konventionellen Marcumar® lässt sich Xarelto® relativ gut steuern und bedarf keiner Injektion, da dieses Medikament in Form von Tabletten eingenommen werden kann.
Auch die regelmäßige Kontrolle der einzelnen Gerinnungsparameter ist bei Xarelto® in der Regel nicht notwendig. Allerdings darf diese Substanz weder bei aktiven Blutungen noch im Rahmen von Schwangerschaft und Stillzeit gegeben werden. Auch bei schwerer Niereninsuffizienz und in Kombination mit anderen gerinnungshemmenden Substanzen ist starke Vorsicht geboten, da sich hierbei ein erhöhtes Blutungsrisiko ergeben kann.
Nach einer Lungenembolie wird Xarelto® meist für die ersten drei Wochen nach dem Ereignis zweimal täglich eingenommen, danach nur noch einmal täglich bis zum Absetzen des Medikaments.
Lesen Sie auch:
Clexane®
Unter Clexane® versteht man den Handelsnamen für Enoxaparin, einem niedermolekularen Heparin.
Wie alle Heparine dieser Gruppe muss auch Clexane® subkutan ein- bis zweimal täglich gespritzt werden und wird in der Regel nach dem Körpergewicht dosiert. Besondere Vorsicht ist bei schwerer Nieren- oder Leberinsuffizienz geboten, hier ist meist eine Dosisanpassung erforderlich.
Ansonsten ist diese Substanz in der Regel gut verträglich und wird auch in Schwangerschaft und Stillzeit eingesetzt.
Dauer der Therapie
Je nach Ausmaß der Verlegung von Lungengefäßen durch das Gerinnsel haben die Betroffenen starke oder weniger starke Beschwerden. Meist geht eine Lungenembolie jedoch mit akuter Luftnot einher und bedarf einer stationären Therapie. Im Krankenhaus wird abhängig von verschiedenen Risikofaktoren in der Regel eine blutgerinnungshemmende Therapie eingeleitet, die meist drei bis sechs Monate weitergeführt werden sollte, um Rezidive zu vermeiden.
Die Akutbehandlung im Krankenhaus beläuft sich meist auf ein bis zwei Wochen, vorausgesetzt es treten keine weiteren Komplikationen ein. Ein wichtiger Grund für die stationäre Behandlung ist die Überwachung der Herzfunktion, die in den meisten Fällen notwendig ist, da es durch eine Lungenembolie meist zu einer akuten Mehrbelastung des rechten Herzens kommt. Aber auch bildgebende Verfahren und Laborkontrollen lassen sich meist nur im stationären Setting durchführen.
Wir empfehlen Ihnen auch unsere Seite zu:
Therapie einer Lungenembolie in der Schwangerschaft
Aufgrund zahlreicher hormoneller Umstellungen im Körper einer werdenden Mutter geht eine Schwangerschaft prinzipiell schon mit einem erhöhten Risiko für die Entstehung einer Lungenembolie einher.
Je nach Quelle wird eine drei- bis vierfache Erhöhung des Risikos angegeben. Bei der Diagnostik einer Lungenembolie ergeben sich bei einer schwangeren Patientin insofern Schwierigkeiten, dass man das Ungeborene möglichst keiner Strahlung aussetzen möchte, das CT in der Regel aber den Goldstandard darstellt.
Bei Schwangeren greift man daher oft auf eine Ultraschalldarstellung der tiefen Beinvenen zurück, dem häufigsten Entstehungsort für Thromben.
Bei der Antikoagulation sollte sichergestellt werden, dass diese über die gesamte Dauer der Schwangerschaft aufrechterhalten wird und mindestens drei Monate lang ist. Mittel der Wahl sind dabei niedermolekulare Heparine wie Clexane®
Diese können auch während einer Schwangerschaft problemlos verabreicht werden. Alternativ kann auch Fondaparinux gegeben werden, ein synthetisches Heparin. Marcumar® ist eigentllich kontraindiziert und sollte nur unter strenger Indikationsstellung und bei Versagen anderer Therapieoptionen eingesetzt werden.
Absolut kontraindiziert in der Schwangerschaft sind neue orale direkte Antikoagulantien wie Xarelto®. Diese sollten bei schwangeren Patientinnen nicht eingesetzt werden. Wenn möglich, sollte auch keine Lysetherapie erfolgen da diese das Blutungsrisiko für die Mutter und für das Ungeborene wesentlich erhöht und zu schweren Komplikationen führen kann. Interventionelle Verfahren mithilfe von Kathetern zur Wiedereröffnung des betroffenen Gefäßes sollten in diesem Fall vorgezogen werden.
Lesen Sie mehr zum Thema:
Weitere Informationen
Lesen Sie auch: