Das Glioblastoma multiforme macht 25% aller primären Hirntumoren aus. Es ist hoch maligne, oft mit infiltrierendem, an mehreren Orten auftretendem (multifokalem) Wachstum in den Großhirnhemisphären, gelegentlich beiderseits über den Balken (Schmetterlingsgliom). Durch die Bildung pathologischer Gefäße neigt der Tumor zu Einblutungen, was zu einem apoplektischen Gliom führt. Symptome sind Kopfschmerzen, Übelkeit, Lähmungen, psychische Veränderungen und epileptische Anfälle.
Inhaltsverzeichnis
- Glioblastom
- Synonym
- Einleitung
- Häufigkeit
- Vorkommen
- Aussehen
- Ursachen
- Risikofaktoren für ein Glioblastom
- Symptome
- Diagnose
- MRT vom Gehirn – Was sieht man?
- WHO - Grade
- Grad 1 und 2
- Grad 3
- Grad 4
- Lebenserwartung / Prognose
- Wie ist der Krankheitsverlauf eines Glioblastoms?
- Wie sieht das Endstadium aus?
- Metastasen
- Wesensveränderungen durch den Tumor
- Kann man ein Glioblastom heilen?
- Was ist ein multiformes Glioblastom?
- Therapie
- Wer kann operiert werden?
- Bestrahlung
- Chemotherapie
- Immuntherapie
- Methadon
- Wann braucht man Cortison?
- Epilepsie
- Ist ein Glioblastom vererbbar?
- Weiterführende Informationen
Glioblastom
Synonym
Glioblastoma multiforme
Einleitung
Das Glioblastom ist der häufigste bösartige (maligne) Hirntumor bei Erwachsenen, der aufgrund seiner sehr schlechten Prognose nach der WHO-Klassifikation der primären Tumore des Zentralnervensystems als schwersten Grad, also ein Glioblastom Grad IV,
eingestuft wird. Das Glioblastom gehört zu den astrozytären Tumoren (Gliome), die feingeweblich (histologisch) den Zellen des Stützgewebes (Gliazellen) des Gehirns ähneln. Gliome enwickeln sich aus den Vorläuferzellen der Gliazellen und sind somit hirneigene Tumore (primäre Hirntumore).

Häufigkeit
Das Glioblastom ist der häufigste bösartige Hirntumor im Erwachsenenalter. Die Häufigkeit von Hirntumoren generell soll bei etwa 50 pro 100.000 Einwohner und Jahr liegen, unter den primären Hirntumoren sind die Gliome mit 4–5 Neuerkrankungen pro 100.000 Einwohner und Jahr am häufigsten. Das häufigste Gliom ist mit über 50% das Glioblastom und macht ca. 25% aller primärer Hirntumoren aus. Somit beträgt die Anzahl der Neuerkrankungen an einem Glioblastom ca. 3 pro 100.000 Einwohner und Jahr.
Am häufigsten tritt er zwischen dem 60 und 70 Lebensjahr auf. Allerdings sind auch deutlich jüngere Menschen betroffen. Männer erkranken fast doppelt so häufig wie Frauen. Bei Kindern sind Glioblastome sehr selten. Im Vergleich zu anderen Tumoren sind Gehirntumore aber zum Glück selten. Nur rund 2% aller Krebskranken leiden an einem Gehirntumor.
Vorkommen
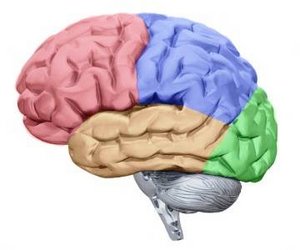
Glioblastome wachsen überall im Zentralnervensystem (ZNS), vor allem aber im Großhirn. Sie gehen von dem Teil des Gehirns aus, das aus Nervenfasern besteht (weiße Substanz). Die Tumore wachsen infiltrierend, meist unter der Großhirnrinde (subkortikal), können aber auch die Rinde ergreifen. Sie finden sich in allen Hirnlappen, aber auch im sogenannten Balken, der die beiden Gehirnhälften (Hemisphären) miteinander verbindet. Ein Glioblastom, das sich von dem Balken (Corpus callosum) aus beiderseits in die vorderen Hirngebiete (Frontallappen) ausbreitet, wird Schmetterlingsgliom genannt. Kommt es zu einer weiträumigen Infiltration des Hirngewebes mit Befall von mindestens zwei Hirnlappen, so spricht man von einer Gliomatosis cerebri. Manchmal wachsen Glioblastome auch entlang des Gewölbes (Fornix), das unter dem Balken liegt, im Thalamus und selten auch im mittleren Hirnstamm.
Aussehen

Mikroskopisch ist das Glioblastom durch vielgestaltige (multiforme) Zellen unterschiedlicher Größe und Form mit eigenartigen Kernen charakterisiert. Sehr viele der Zellen befinden sich in der Zellkernteilung (Mitose). Durch das schnelle Wachstum des Tumors und der Ausschüttung eines gefäßbildenden Faktors, der von dem Tumorgewebe produziert wird, kommt es zur Neubildung von abnormen (pathologischen) Gefäßen mit defekter Wandstruktur. Dadurch kommt es zu kleinen Gefäßausweitungen (Aneurysmen und Varizen), Kurzschlüssen von Arterien und Venen (arteriovenöse Anastomosen) und sogenannten „frühen Venen“. Dies führt oftmals zu Blutungen (apoplektisches Gliom) und zu einer mangelhaften Ernährung des Tumors, was zu einem Absterben von aktiven Zellen (Nekrose) innerhalb des Tumors führt. Diese nekrotischen Tumorbereiche sind häufig von Pseudopallisaden umgeben, die aus linear angeordneten neubildenden (neoplastischen) Zellen bestehen.
Zusätzlich entwickelt sich eine Schwellung des Gewebes aufgrund einer Einlagerung von Flüssigkeit aus dem Gefäßsystem um den Tumor herum (peritumorales Ödem), die oft zu einer Schwellung der ganzen Gehirnhälfte führt.
Ursachen
Ein Glioblastom kann primär (meist ältere Patienten), aber auch sekundär durch fortschreitendes Wachstum (Progression) eines Astrozytoms des WHO Grades III entstehen (meist Patienten mittleren Alters). Astrozytome entwickeln sich aus bestimmten Gliazellen, den Astrozyten, und gehören wie Glioblastome zu den Gliomen.
Die Rolle der genetischen Faktoren bei der Entstehung von Hirntumoren ist in den letzten Jahren immer mehr in den Vordergrund getreten. Patienten mit sekundären Glioblastomen haben als Hauptunterscheidungsmerkmal eine Veränderung des Proteins p53 (p53-Mutation), das den Zellzyklus kontrolliert (Tumorsuppressor), und einen Verlust von Genen (Allelverlust) auf dem Chromosom 17. Außerdem sind sie 10 bis 20 Jahre jünger als Patienten mit primärem Glioblastom, bei denen typischerweise eine EGF-Rezeptor-Gen-Vervielfältigung (Amplifikation) bzw. eine übermäßige Produktion (Überexpression) des EGF-Rezeptors vorliegt. Der EGF-Rezeptor dient als Andockstelle für den Epidermalen Wachstumsfaktor (Epidermal Growth Factor), der als Signalmolekül im Zellzyklus auftritt. Glioblastome sind genetisch sehr unterschiedlich (heterogen) und haben in ca. 20% einen Verlust eines Gens (Deletionen) und in gut 50% Genvervielfältigungen. Häufigster Befund ist ein Genverlust auf dem Chromosom 10 in drei Viertel der Fälle.
Für die Mehrzahl der Hirntumoren spielen genetische Faktoren jedoch keine Rolle. Auch Umweltfaktoren spielen nur eine untergeordnete Rolle. Als Beispiel für einen beeinflussenden Umweltfaktor lässt sich das Vinylchlorid in dem Plastik PVC nennen. Ein vererbbarer genetischer Faktor lässt sich bei den seltenen erblichen Erkrankungen Li-Fraumeni-Syndrom und Turcot Syndrom beobachten. Hier treten Glioblastome familiär gehäuft auf.
Risikofaktoren für ein Glioblastom
Die Ursachen für ein Glioblastom sind nicht vollständig erforscht. Die allermeisten Glioblastome entstehen spontan, also zufällig. Eine hohe Strahlenbelastung konnte jedoch als Risikofaktor identifiziert werden. Es gibt auch seltene genetische Erkrankungen, bei denen die Betroffenen generell ein erhöhtes Risiko für Tumore haben, z.B. das Li-Fraumeni-Syndrom. Erkrankungen dieser Art gelten auch als Risikofaktor ein Glioblastom zu entwickeln. Darüber hinaus ist es auch nicht selten, dass Hirntumore Grad 3 im Verlauf auch bösartiger werden und sich so ein Glioblastom (Grad 4) entwickeln kann. Diesen Prozess nennt man maligne Progression. Auf Basis von einem anderen Gehirntumor kann sich auch unter Therapie ein Glioblastom entwickeln. Man spricht dann in der Fachsprache von einem sekundären Glioblastom.
Symptome
Die ersten klinischen Symptome treten nach wenigen Wochen oder auch früher auf. Kopfschmerzen (35%), epileptische Anfälle (30%) und psychische Veränderungen (16%) sind dabei die häufigsten Erstsymptome. Ein erhöhter Hirndruck aufgrund des raumfordernden Effekts des Tumors und der damit verbundenen Störung des Hirnwasserflusses (Liquorzirkulation) verursachen Kopfschmerzen, Übelkeit, Erbrechen und eine Schwellung (Ödem) der Austrittsstelle des Sehnervs (Stauungspapille), was zu Sehstörungen führen kann. Lähmungen können ebenfalls durch die Ausdehnung des Tumors auftreten. Anfallsartige Verschlechterungen der Symptome sind auf eine Tumoreinblutung zurückzuführen (apoplektisches Gliom) und sind nicht selten.
Weitere Informationen finden Sie auch unter unserem Thema: Gehirntumor Anzeichen.
Diagnose
In der Computertomographie (CT) zeichnen sich Glioblastome durch eine unterschiedliche Dichte, unscharfe Tumorbegrenzung, einer zentralen Nekrose innerhalb des Tumors und ein großes Ödem um den Tumor herum (peritumorales Ödem) aus. Nach Gabe des Kontrastmittels, einem Stoff, der den Bildkontrast erhöht, kommt es vor allem in der Randzone des Tumors zu einer Ansammlung (Anreicherung) des Kontrastmittels. Bei kleinen Tumoren wird so eine Ringstruktur, bei größeren eine Girlandenformation sichtbar. Tumoreinblutungen sind bei ca. 7% der Glioblastome zu sehen.
In dem MRT vom Gehirn sieht man die Ausbreitung des Tumors, zum Teil über den Balken hinweg. Nach Kontrastmittelgabe reichert sich das Kontrastmittel in den soliden Tumoranteilen an. Zum typischen MRT-Bild des Glioblastoms gehören zusätzlich Blutungsreste und ein ausgedehntes, fingerförmiges peritumorales Ödem. Die Abgrenzung von einer großen, nekrotischen Hirnmetastase und von einem Hirnabszess kann jedoch schwierig sein.
Eine Angiographie kann zusätzlich durchgeführt werden, ist heute aber kein Standard mehr in der Diagnostik von Glioblastomen. Dabei wird Kontrastmittel in die Blutgefäße injiziert und die Gefäße werden mittels diagnostischer Bildgebungsverfahren wie Röntgen oder MRT dargestellt. Die Angiographie bei Glioblastomen lässt bei 60–70% eine Anreicherung des Kontrastmittels in den pathologischen Gefäßen erkennen. Die aus dem Tumor ableitenden Venen werden schon während der arteriellen Phase dargestellt (»frühe Venen«), was den zu schnellen Fluss des Blutes in die Venen durch die arteriovenösen Anastomosen zeigt.
Lesen Sie hier mehr zu dem Thema Angiographie
Die endgültige Artdiagnose eines Tumors wird feingeweblich (histologisch) gestellt. Bei vielen nichtoperablen Tumoren ist vor Bestrahlung eine histologische Sicherung der Tumorart erwünscht. Die Hirnbiopsie, bei der ein sehr kleines Stück des Gehirngewebes herausgeschnitten wird, wird entweder offen gleichzeitig mit einer Tumorverkleinerung oder in lokaler Anästhesie minimalinvasiv, also mit der kleinsten Verletzung, durchgeführt.
Das könnte Sie auch interessieren: Hirnbiopsie und Glioblastom in Endstadium
MRT vom Gehirn – Was sieht man?
Der Verdacht auf ein Glioblastom wird oft mittels eines bildgebenden Verfahrens gestellt. Meistens ist dies die Magnetresonanztomografie. Der typische Befund zeigt einen Tumor ohne homogene (gleichmäßige) Struktur. Die soliden Anteile (feste Anteile) sind sehr gut durchblutet und nehmen daher viel Kontrastmittel auf. Dies fällt auf den ersten Blick auf. Sie sind sehr hell und leuchten förmlich auf dem MRT Bild. Daneben gibt es immer wieder Kontrastmittelaussparungen (Bezirke, die im MRT nicht hell erscheinen). Das sind zystische Anteile oder abgestorbene Zellverbände (Nekrosen), diese werden nicht von einem Blutgefäß versorgt und können daher kein Kontrastmittel aufnehmen. Den Tumor umgehend sieht man meist ein Ödem (aufgeschwollene Zellen). Oft erkennt man schon bei Erstdiagnose den raumfordernden Effekt des Tumors, d.h. die Mittelline ist durch das Tumorwachstum bereits verschoben. Für die endgültige Diagnose muss jedoch eine Probe entnommen werden und diese unter dem Mikroskop untersucht werden. Erst der Pathologe kann die Diagnose eines Glioblastoms also sicher bestätigen.
Lesen Sie mehr unter: MRT vom Gehirn
WHO - Grade
Die Weltgesundheitsorganisation (WHO) teilt Gehirntumore anhand ihres Wachstumsverhaltens in 4 Gruppen ein. Grad 1 Tumore wachsen langsam und gelten als gutartig. Grad 4 Tumore wachsen extrem schnell und haben eine sehr schlechte Prognose. Grad 2 und 3 Tumore liegen dazwischen. Ein Glioblastom ist ein Tumor, der von den Stütz- oder Hüllzellen der Nervenzellen ausgeht, diese werden in der Fachsprache Gliazellen genannt. Daher kommt auch der Name. Aufgrund seines schnellen Wachstums und der schlechten Prognose handelt es sich bei Glioblastomen um Grad 4 Tumore.
Grad 1 und 2
Während Grad 1 Tumore von der WHO als gutartige Hirntumore bezeichnet werden, sind in Grad 2 Tumoren bereits vereinzelt bösartige Zellen nachweisbar. Bei 50% der Grad 2 Tumore entwickelt sich im Verlauf ein neuer Tumor mit einer höheren Bösartigkeitsstufe (Grad 3-4), daher ist die Lebenserwartung auch eingeschränkt. Ähnlich wie das Gliobastom gehen diese Tumore auch von den Stütz- oder Hüllzellen des Gehirns aus. Im Gegensatz zu dem Glioblastom, ein Grad 4 Tumor, wachsen Grad 2 Hirntumore sehr viel langsamer und haben eine deutlich bessere Prognose.
Grad 3
Grad 3 Tumore sind nach der Klassifikation der Weltgesundheitsorganisation (WHO) bösartige Hirntumore mit schnellem Wachstum. Die Prognose ist schlecht. Trotz Therapie versterben viele Patienten nach 2-3 Jahren. Typische Grad 3 Tumore sind sogenannte anaplastische Astrozytome; wie die Glioblastome gegen sie von den Stütz- und Hüllzellen der Nervenzellen aus. Glioblastome sind aufgrund ihres noch rasanteren Wachstums allerdings ein Tumor der Gruppe 4. Trotz Maximaltherapie ist die mittlere Überlebensdauer ca. 1 Jahr.
Grad 4
Grad 4 Tumore sind noch bösartiger, wachsen schneller und führen zu einer deutlichen Reduktion der Lebenserwartung trotz Therapie. Die Einteilung des Tumors in den entsprechenden WHO Grad beeinflusst daher stark die Prognose des Patienten. Glioblastome sind immer Grad 4 Tumore mit einer sehr schlechten Prognose. Natürlich spielen auch noch andere Faktoren wie Operabilität, Lokalisation sowie das Ansprechen auf Chemo- und/oder Strahlentherapie eine wichtige Rolle, wenn es um die Prognose des Patienten geht. Die mittlere Überlebensdauer bei einem Glioblastom liegt im Durchschnitt bei einem Jahr nach Diagnosestellung.
Lesen Sie mehr unter: Glioblastiom Grad 4
Lebenserwartung / Prognose
Das Glioblastom ist leider sehr schwierig zu behandeln. Eine dauerhafte Heilung ist normalerweise nicht möglich. Letzten Endes versterben die Patienten meist an dem Tumor. Die Standardtherapie besteht aus Operation mit anschließend Bestrahlung und Chemotherapie. Leider wächst der Tumor sehr schnell und infiltriert das umliegende Nervengewebe, so dass bei einer Operation nie alle Tumorzellen entfernt werden können. Der Tumor kommt meist zurück (Rezidiv). Bei den nachfolgenden Zahlen zur Prognose und Lebenserwartung sollte man sich bewusst machen, dass es sich um Statistiken handelt, im Einzelfall kann die tatsächliche Überlebenszeit des Patienten weit davon abweichen.
Die beste Prognose haben junge Patienten (Alter < 50 Jahre) mit gutem Operationsergebnis. 70% überleben das erste Jahr. Die mittlere Überlebensdauer nach Diagnosestellung ist 17-20 Monate. Nur ca. 15 Prozent sind nach 5 Jahren noch am Leben. Mit zunehmendem Alter verschlechtert sich die Prognose. Bei Patienten über 50 Jahren oder bei jüngeren Patienten mit deutlichen Einschränkungen ist die mittlere Überlebensdauer trotz gutem Operationsergebnis oft nur knapp ein Jahr. Bei Patienten ohne operativen Eingriff oder mit einer schlechten neurologischen Funktion postoperativ ist die Prognose noch schlechter. Nur ein Drittel überlebt das erste Jahr. Der Durchschnitt verstirbt nach 8 Monaten. Einzelne Patienten haben trotz Rezidiv eine relativ gute Lebensqualität und überleben dessen ungeachtet mehrere Jahre. Dabei handelt es sich aber bisher um Einzelfälle. Welche Faktoren die Prognose günstig beeinflussen wird daher intensiv erforscht.
Lesen Sie mehr zum Thema: Glioblastom - Verlauf der einzelnen Stadien
Wie ist der Krankheitsverlauf eines Glioblastoms?
Das Glioblastom ist ein bösartiger Tumor im Gehirn mit einer sehr schlechten Prognose. Eine Heilung ist in der Regel nicht möglich. Die Patienten versterben im Schnitt ca. 1 Jahr nach Diagnosestellung. Ist die Lage des Tumors günstig und der Allgemeinzustand des Patienten gut, erfolgt zunächst eine operative Entfernung. Leider wächst das Glioblastom so infiltrierend in das Nervengewebe, dass nie alle Tumorzellen entfernt werden können. Der Operation schließt sich deshalb eine Bestrahlung sowie eine Chemotherapie an. Dadurch kann man den natürlichen Verlauf der Erkrankung jedoch nur verzögern. Außer in seltenen Einzelfällen kehrt der Tumor wieder zurück (Rezidiv). Meist wächst er so schnell, dass sich durch den erhöhten Druck auf das Gehirn bald Symptome entwickeln wie Übelkeit/Erbrechen und starke Kopfschmerzen. Es folgen Bewusstseinsstörungen. Durch den steigenden Hirndruck kommt es dann letzten Endes zu einer Einklemmung bestimmter Hirnregionen. Ist der Hirnstamm betroffen, sind Atemlähmung und Tod die Folge. Durch die oben genannte Behandlung kann dies für einige Monate verzögert werden, der Verlauf der Erkrankung ist jedoch nicht aufzuhalten und endet mit dem Tod.
Lesen Sie mehr zum Thema unter: Verlauf eines Glioblastoms
Wie sieht das Endstadium aus?
Das Glioblastom ist ein bösartiger Tumor, an dem die Patienten in der Regel versterben. Eine Heilung ist aktuell nicht möglich – trotz Operation, Bestrahlung und Chemotherapie. Letzten Endes ist es schwierig festzulegen, wann das Endstadium erreicht ist. Meist kommt es nach der Operation erneut zum Wachstum des Tumors (Rezidiv). Dieser ist oft nicht mehr operabel. Manchmal ist der Tumor bereits bei Diagnosestellung so groß oder ungünstig lokalisiert, dass er gar nicht operabel ist. Als Grad 4 Tumor zeichnet sich das Glioblastom durch ein rasantes Wachstum aus. Im Endstadium ist der Tumor also sehr groß. Im knöchernen Schädel ist allerdings nur begrenzt Platz. Der Druck auf das Gehirn steigt. Bei erhöhtem Hirndruck leiden die Patienten dann unter Übelkeit und Erbrechen sowie schlimmen Kopfschmerzen. Auch Bewusstseinsstörungen bis zum Koma sind möglich. Die Patienten sind oft schläfrig und verwirrt. Aufgrund des steigenden Hirndrucks besteht auch die Gefahr dass bestimmte Hirnregionen durch zu viel Druck im Schädel eingeklemmt werden, ist das Atemzentrum im Hirnstamm beispielsweise davon betroffen, kommt es zur Atemlähmung und zum Tod.
Lesen Sie mehr zum Thema: Erhöhter Hirndruck - Anzeichen, Ursachen und Behandlung
Wie bei den meisten Krebserkrankungen in Endstadium sind die Patienten oft durch die lange Krankheitsdauer ausgezehrt. Sie fühlen sich schlapp und erschöpft, können vielleicht nicht mal mehr das Bett verlassen. Man versucht dann das Leid etwas zu lindern, indem man dem Patienten starke Schmerzmittel verordnet. Auch Medikamente gegen die Übelkeit bekommt der Patient. Eine palliativmedizinische Betreuung sollte erfolgen.
Das könnte Sie auch interessieren: Glioblastom in Endstadium
Metastasen
Metastasen verbreiten den Krebs im ganzen Körper. Man hört auch oft die Worte der Tumor hat gestreut. Man spricht davon, wenn der Tumor in einem anderen Teil des Körpers Tochtergeschwulste gebildet hat. Beim Glioblastom handelt es sich um einen schnell wachsenden bösartigen Hirntumor. Es wächst infiltrativ, d.h. es breitet sich sowohl im Gehirn als auch in den Hirnhäuten aus. Über das Nervenwasser (Liquor) verteilen sich die Tumorzellen im gesamten zentralen Nervensystem (Gehirn und Rückenmark) und können sich überall wieder neu ansiedeln. Außerhalb des zentralen Nervensystems bilden sich selten Tochtergeschwülste.
Wesensveränderungen durch den Tumor
Jede Krebserkrankung stellt im Leben des Betroffenen einen deutlichen Einschnitt da. Die Verarbeitung der Diagnose Glioblastom ist individuell sehr verschieden, aber alleine diese Diagnose ist eine massive psychische Belastung. Die plötzliche Konfrontation mit der Tatsache, dass das eigene Leben endlich ist, verändert die meisten Menschen. Zudem ist die Persönlichkeit im Gehirn gespeichert, v.a. im vorderen Teil des Gehirnes, dem sog. Frontallappen. Tumore die dort wachsen können zu organischen Wesensveränderungen führen, da sie das eigene Hirngewebe verdrängen. Leider sind die Patienten meist grundlos aggressiv und beleidigend. Das ist für das Umfeld eine extreme Belastung. Durch den steigenden Hirndruck im Endstadium der Erkrankung sind die Patienten dann meist antriebslos und müde.
Kann man ein Glioblastom heilen?
Diese Frage muss leider mit einem klaren Nein beantwortet werden. Die mittlere Überlebensdauer nach Diagnosestellung ist ein Jahr. Natürlich kann der einzelne Fall erheblich von der Statistik abweichen. Gerade junge Patienten (unter 50 Jahren) haben eine etwas bessere Prognose. Sie überleben im Schnitt ca. 18 Monate. Vereinzelt gibt es auch wieder Patienten, die nach 5 Jahren noch am Leben sind. Dass es weltweit vereinzelt Patienten gibt, die 10 Jahre nach Diagnosestellung noch leben, ist möglich, aber sicher die absolute Ausnahme. Zum jetzigen Stand der Wissenschaft ist eine Heilung des Glioblastoms nicht möglich. Es werden zahlreiche Forschungsansätze verfolgt, bis jetzt ist es jedoch eher unwahrscheinlich, dass in den nächsten Jahren eine so bahnbrechende Therapie entdeckt wird, die zu einer Heilung des Tumors führen könnte. In allen Studien konnte bisher lediglich eine Verlängerung der Überlebenszeit in Monaten erreicht werden.
Was ist ein multiformes Glioblastom?
Der Begriff multiform bedeutet wörtlich übersetzt „vielgestaltig“, d.h. auf den Tumor bezogen, dass der Tumor durch eine vielfältige Erscheinung gekennzeichnet ist. Dieser Begriff kommt aus der Pathologie. Bereits im MRT Bild kann jedoch auch der unerfahrene Arzt sehen, dass der Tumor keine gleichmäßige Struktur hat. Unter dem Mikroskop sieht man dann Einblutungen und Nekrosen (=abgestorbene Zellen). Jedes Glioblastom ist per Definition ein multiformer Tumor. Dies inhomogene (ungleichmäßige) Zusammensetzung charakterisiert das Glioblastom.
Therapie
Die Therapie besteht in der möglichst radikalen operativen Tumorentfernung und der anschließenden Bestrahlung mit 60 Gray Gesamtdosis (30 Einzelfraktionen – 2 Gy/5 Tage/Woche für 6 Wochen). Das Ödem spricht gut auf die Behandlung mit Steroiden, zum Beispiel Dexamethason, an. Unter Bestrahlung und antiödematöser Therapie kann zunächst eine klinisch eindrucksvolle Besserung eintreten. Ein erneutes Auftreten bzw. Wachstum (Rezidiv) des Tumors ist aber unvermeidlich. Als wesentliche prognostische Faktoren gelten: Lebensalter und Ausmaß der klinischen Beeinträchtigung zu Beginn der Therapie.
Auch Chemotherapie wird zunehmend mit der Bestrahlung, besonders mit der Substanz Temozolomid, kombiniert oder nachfolgend eingesetzt. Dennoch sind die Therapiechancen bei Gliompatienten gering, die Einjahresüberlebensrate liegt beim Glioblastoma multiforme bei 30–40%. Die Chemotherapie mit Nitroseharnstoffen (BCNU, CCNU) führt zu einer geringen Lebensverlängerung von nur wenigen Wochen bis Monate. Eine Alternative zu den Nitroseharnstoffen ist das Temozolomid, das geringere Nebenwirkungen aufweist und als orales Zytostatikum, ein die Zellteilung hemmendes Mittel, ambulant verabreicht werden kann. Die kombinierte Strahlen- und Chemotherapie mit Temozolomid führt zu einer Lebenszeitverlängerung auf 14 Monate (ohne Temozolomid: 12 Monate) sowie einer erhöhten Zweijahresüberlebensrate von 26% (ohne: 10%). Von dieser Therapie scheinen junge Patienten unter 45 Jahre in gutem gesundheitlichem Zustand am ehesten zu profitieren.
Temozolomid wird auch bei der Rezidivtherapie bösartiger Gliome angewandt. Die Rezidivtherapie führt bei etwa 50% der Patienten zu einer Stabilisierung des Tumorwachstums und zu einer Gesamtüberlebenszeit von 13 Monaten nach Beginn der Rezidivtherapie.
Wer kann operiert werden?
Für eine operative Entfernung eines Glioblastoms entscheidet man sich wenn der Tumor aufgrund seiner Lage gut zugänglich und entfernbar ist. Meist gibt es schon Hinweise auf das schnelle Wachstum des Tumors; man sieht in der Schnittbildgebung dass umgebendes Gewebe verdrängt wird. Man nennt dies einen raumfordernden Effekt. Nicht zuletzt ist auch der Allgemeinzustand bzw. die Narkosefähigkeit des Patienten für die Entscheidung zu einer Operation ausschlaggebend. Nicht operiert werden können Tumore, die zu nah an wichtigen Hirnregionen liegen. Ist zum Beispiel das Sprach- oder das Atemzentrum direkt neben dem Tumor, ist eine Operation nicht möglich bzw. sinnvoll. Dann gilt der Tumor als inoperabel.
Bestrahlung
Durch eine Operation können nie alle Tumorzellen entfernt werden, d.h. vereinzelte Tumorzellen sind noch vorhanden. Diese können wieder zu einem großen Tumor wachsen. Um dies zu verhindern oder zumindest möglichst viele verbliebene Tumorzellen abzutöten schließt sich nach der Operation eine Bestrahlung an. Dabei wird nicht nur die ursprüngliche Tumorregion bestrahlt, sondern auch ein Sicherheitssaum von 2-3 cm. Manchmal erhält der Patient parallel zur Bestrahlung auch eine Chemotherapie.
Lesen Sie mehr zum Thema: Behandlung durch eine Strahlentherapie
Chemotherapie
Neben der Operation und der Bestrahlung gehört die Chemotherapie zur Standardtherapie bei Glioblastomen. Da der Tumor infiltrativ ins Hirngewebe wöchst, können bei der Operation nie alle Tumorzellen entfernt werden. Daher kann man mittels Chemotherapie das rezidivfreie Überleben um mindestens ein paar Monate verlängern. Temozolomid ist das Chemotherapeutikum der Wahl. Es kann gut die Blut-Hirn-Schranke überwinden. Es ist in Tablettenform verfügbar und kann zuhause eingenommen werden. Zudem ist es relativ nebenwirkungsarm und gut verträglich.
Immuntherapie
Im Kampf gegen bösartige Tumore werden heutzutage immer mehr Immuntherapeutika eingesetzt. Doch was versteht man eigentlich unter dem Begriff Immuntherapie?
Bei einer Immuntherapie beeinflusst man das körpereigene Immunsystem mittels Medikamenten um Tumorzellen abzutöten. Es ist eigentlich ein Sammelbegriff für zahlreiche unterschiedliche Ansätze. Das Glioblastom ist ein sehr schnell wachsender bösartiger Hirntumor, der trotz Maximaltherapie mit einer sehr schlechten Prognose einhergeht. Daher ruhen viele Hoffnungen auf der Immuntherapie. In diesem Bereich gibt es auch durchaus vielversprechende Ansätze, die aktuell im Rahmen klinischer Studien intensiv erforscht werden.
Methadon
Viele Patienten und Angehörige haben durch Medienberichte über Methadon jetzt neue Hoffnung. Doch was sind die Fakten? Im Labor konnte gezeigt werden, dass durch Methadon Krebszellen besser auf die Chemotherapie ansprechen und dadurch effektiver abgetötet werden.
Eine an der Charité in Berlin durchgeführte Studie an 27 Patienten konnte jedoch keinen Überlebensvorteil zeigen, für die Gruppe, die mit Methadon behandelt wurden. Andere Kollegen berichten jedoch immer wieder von Einzelfällen in denen Patienten mit Methadon 2-3 Jahre länger rezidivfrei leben. Aktuell ist es daher sehr schwierig eine Empfehlung auszusprechen. Erste Laborergebnisse und Einzelfallberichte sprechen für Methadon. Hochwertige klinische Studien mit großen Patientenkollektiven fehlen jedoch bisher. Man kann sicher erst in ca 3 Jahren mit diesen Daten rechnen. Vorher kann man keine wissenschaftlich fundierte Aussage zum Stellenwert von Methadon in der Krebstherapie machen. Betroffene Patienten haben jedoch die Möglichkeit mit ihrem behandelnden Arzt zu besprochen, ob Methadon als off label Therapie nicht trotzdem verordnet werden kann, im Sinne eines experimentellen Heilversuchs. Eine off label Therapie bedeutet dass der Arzt dem Patient ein Medikament verschreibt, obwohl es für die Behandlung einer bestimmten Krankheit garnicht zugelassen ist. Methadon ist ein altes lang erprobtes Medikament. Es hat bisher jedoch keine Zulassung zur Ergänzung der Chemotherapie beim Glioblastom, weil es bisher keine validen Daten gibt, die dessen Wirksamkeit belegen.
Für mehr Informationen zum Einsatz von Methadon zur Therapie von Sucht lesen sie folgenden Artikel: Therapie einer Sucht
Wann braucht man Cortison?
Wassereinlagerungen (Ödeme) rund um den Tumor sind vor allem im Endstadium eines Glioblastoms oft Teil der Erkrankung. Dies führt zu einem Anschwellen der Nervenzellen und erhöht so den Hirndruck. Damit handelt es sich beim sog. Hirnödem um ein potenziell lebensbedrohliches Krankheitsbild. Um dem Hirnödem entgegenzuwirken braucht man Cortison. Es stabilisiert die Zellwände, die Zellen nehmen nicht mehr unkontrolliert Flüssigkeit auf und verlieren wieder an Größe. Das Hirn schwillt ab. Dies passiert schon innerhalb von wenigen Stunden nach Cortisongabe. Daher ist Cortison ein für den Patienten oft überlebenswichtiges Medikament.
Epilepsie
Die Hälfte aller Patienten mit Glioblastom entwickelt im Verlauf auch epileptische Anfälle. Dabei können die Anfälle manchmal sogar das erste Zeichen des Tumors sein, das zur Diagnose führt. Wird der Tumor dann operativ entfernt, sinkt das Risiko für Anfälle zunächst deutlich ab. Grundsätzlich haben Patienten mit einem Gehirntumor jedoch ein deutlich erhöhtes Epilepsierisiko, daher sollte nach dem ersten Anfall definitiv eine medikamentöse Anfallsprophylaxe begonnen werden, um das Risiko für weitere Anfälle zu senken.
Lesen Sie mehr zum Thema: Gehirntumor anzeichen
Ist ein Glioblastom vererbbar?
In den meisten Fällen ist diese Frage glücklicherweise mit einem klaren Nein zu beantworten. Auch wenn bei einem Verwandten, z.B. einem Elternteil ein Glioblastom aufgetreten ist, hat man selbst kein höheres Risiko an diesem Hirntumor zu erkranken als die Normalbevölkerung. Es handelt sich beim Glioblastom um einen sporadisch auftretenden Tumor, d.h. der Tumor tritt zufällig auf, es gibt keine Hinweise auf Erblichkeit. Es gibt jedoch seltene genetische Erkrankungen bei denen generell ein erhöhtes Risiko für bösartige Tumoren besteht, z.B. das Li-Fraumeni-Syndrom oder das Turcot-Syndrom. Bei betroffenen Familien können dann natürlich auch gehäuft Glioblastome auftreten.
Weiterführende Informationen
Weitere Informationen zum Thema Glioblastom finden Sie hier:
Eine Übersicht der bisher erschienenen Themen der Neurologie finden Sie unter Neurologie A-Z.